À 750°C, l’argent ne s’efface pas : il change. Les métaux précieux, loin de l’image d’inaltérabilité qu’on leur prête parfois, révèlent sous la flamme ou la soudure des réactions complexes, des transformations de surface qui intriguent autant qu’elles inquiètent les bijoutiers et orfèvres. Derrière l’éclat du métal, il y a toute une mécanique d’atomes et d’oxygène, de feu et de chimie, qui façonne la matière et la couleur.
Comment s’oxydent les alliages d’or et d’argent ?
Les alliages d’or et d’argent nécessitent souvent des températures élevées, entre 600 et 800°C, pour leur mise en forme. C’est le cas lorsqu’il s’agit de restaurer leur malléabilité après un durcissement par traction, ou lors des opérations de brasage et de soudage.
Généralement, ces traitements se font à l’air libre, sans précautions particulières. Résultat, une couche d’oxyde se forme à la surface du métal. Pour un alliage d’or, on élimine cet oxyde par décapage dans une solution acide (retrouvez nos produits de roche ici). Mais on le remarque vite : l’or rose, par exemple, vire au jaune. Sur l’argent 1er titre utilisé en orfèvrerie, ce sont des taches sombres, les fameuses « taches de feu », qui apparaissent. Les autres alliages d’argent réagissent aussi, mais selon des modalités différentes.
Pourquoi ces phénomènes d’oxydation ? Comment les éviter, ou au moins limiter leurs effets ? C’est ce que nous allons explorer ici, sans jargon inutile, mais sans éluder la réalité technique.
Diffusion dans les solides
Derrière l’oxydation, il y a d’abord un principe physique : la diffusion. Les atomes, même à l’état solide, se déplacent, surtout dans les alliages. Quand des zones présentent des concentrations différentes, les atomes migrent des régions les plus riches vers les plus pauvres, cherchant un équilibre.
Un exemple concret : si l’on recouvre un objet en or fin d’une fine couche d’argent par électrolyse, puis qu’on le chauffe, l’aspect change radicalement. Le blanc argenté devient verdâtre. À la surface, un alliage or-argent s’est formé : l’argent pénètre l’or, pendant que l’or fait le chemin inverse. Ce même processus se produit si deux alliages différents sont soudés l’un à l’autre. La diffusion tend à uniformiser la composition des alliages, modifiant parfois, de façon inattendue, leur aspect extérieur.
Oxydation
L’oxydation, c’est la réaction du métal avec l’oxygène, en général, celui de l’air, pour former un oxyde. Chauffez du cuivre à l’air libre : il passe du rouge (oxydule) au noir (oxyde). L’or pur et l’argent, eux, ne changent pas d’apparence. Ils résistent à la formation d’oxydes visibles. L’argent, cependant, a cette singularité : il dissout l’oxygène, qui diffuse de la surface vers l’intérieur. Cela aura son importance par la suite.
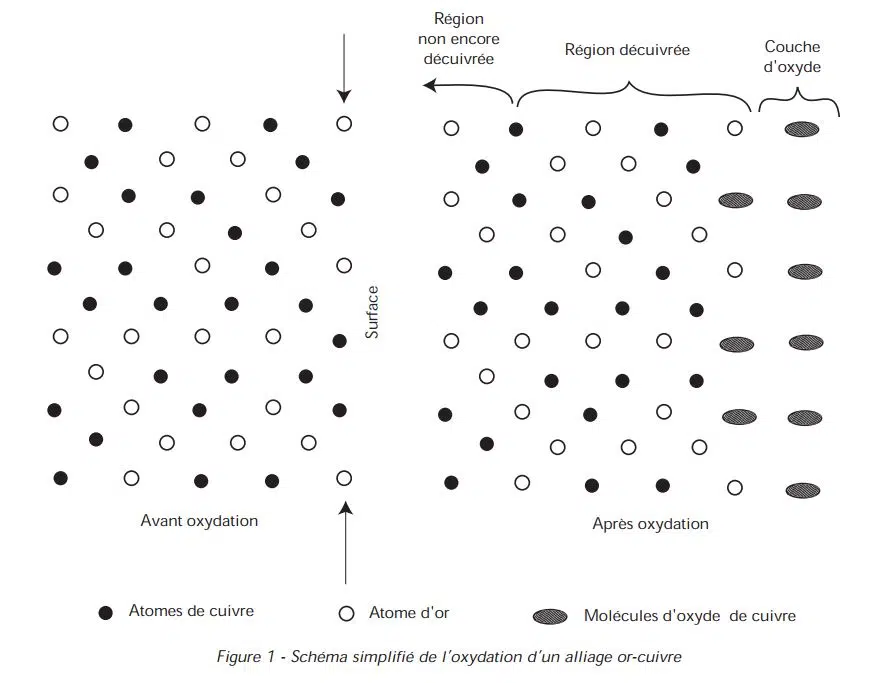
L’or pur ne s’oxyde pas. Le cuivre, lui, s’oxyde très facilement. Dans un alliage or-cuivre chauffé à l’air, le cuivre de surface réagit avec l’oxygène et se transforme en oxyde. Cette réaction crée une surface appauvrie en cuivre : le cuivre de l’intérieur migre alors vers la surface, où il est à son tour oxydé. Le métal agit comme une pompe, attirant le cuivre en surface pour être consommé par l’oxygène.
Arrêtons l’expérience et coupons l’alliage or-cuivre : voilà ce qu’on observe, couche par couche :
- En surface, une pellicule d’oxyde s’est formée.
- Juste en-dessous, la zone est totalement dépourvue de cuivre libre.
- En profondeur, la concentration de cuivre augmente progressivement, jusqu’à retrouver la teneur initiale.
Si on retire l’oxyde formé, la surface dévoile alors la teinte de l’or pur.
Spécificités des alliages or, argent et cuivre
Dans un alliage or-argent-cuivre, typiquement un or rose 18 carats, le scénario se répète : le cuivre s’oxyde et disparaît en surface. Après décapage, la couleur devient plus jaune. Un polissage permet de retirer la couche superficielle appauvrie et de retrouver l’aspect initial de l’alliage (voir Figure 1). Pour ne pas subir cette altération de couleur, il faut empêcher l’oxydation du cuivre en surface, donc travailler dans une atmosphère sans oxygène.
Dans l’industrie, on utilise des fours de recuit équipés d’ambiances protectrices à base d’azote, d’hydrogène ou de dioxyde de carbone. Une méthode artisanale : placer les pièces dans des boîtes en fer remplies de copeaux de fonte, qui capturent l’oxygène avant qu’il ne touche le cuivre. Pour le brasage ou la soudure, des flux comme le borax ou l’acide borique (ou mieux, des torches alimentées par des gaz contenant de l’acide borique) créent une mince couche protectrice fondue sur la pièce.
Le cas de l’argent
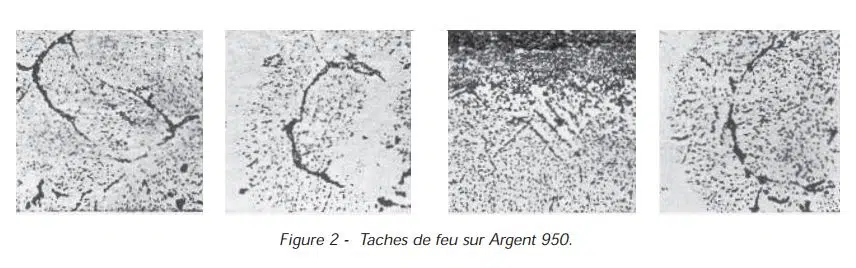
L’argent, on l’a vu, dissout l’oxygène. Chauffé à l’air, il ne noircit pas, mais l’oxygène s’infiltre lentement vers l’intérieur du métal. Pour les alliages argent-cuivre, deux phénomènes de diffusion cohabitent : le cuivre migre de la surface vers l’intérieur, l’oxygène fait le chemin inverse. Si le cuivre migre plus vite, une couche d’oxyde se forme en surface. Si c’est l’oxygène qui l’emporte, il s’enfonce dans l’alliage et oxyde le cuivre à l’intérieur : c’est l’« oxydation interne ». Au microscope, on observe les grains d’oxyde qui se sont formés à l’intérieur du métal (voir Figure 2).
À l’extérieur, l’argent prend une teinte sombre, marquée par des taches de feu. Plus l’alliage contient de cuivre, plus la couche d’oxyde en surface est épaisse, comme sur l’argent à 835 ‰. Sur des alliages plus dilués, comme l’argent premier titre, des taches internes se forment par oxydation interne.
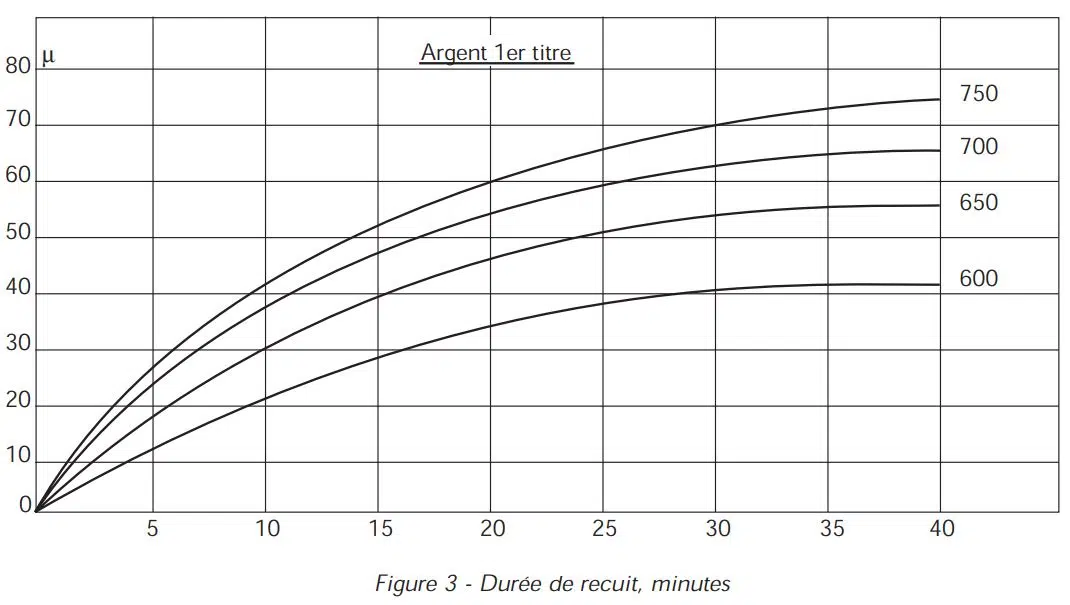
Les observations menées au laboratoire Cookson-CLAL ont permis de tracer des courbes (Figure 3) qui relient la profondeur de pénétration de l’oxygène, et donc la gravité des taches de feu, à la température et au temps de chauffage. Par exemple, dix minutes à 750°C suffisent à créer une tache de feu de 42 microns (0,042 mm) sur de l’argent 1er titre.
Que faire contre les taches de feu de l’argent ?
Pour contrer les taches de feu de l’argent 1er titre, il existe plusieurs approches :
- La prévention : utiliser une atmosphère ou une protection adaptée pour éviter l’oxydation (voir plus haut pour les solutions employées avec les alliages d’or).
- Le camouflage : masquer la tache de feu par un dépôt galvanique d’argent fin (Retrouvez notre gamme pour la galvanoplastie).
- La correction mécanique : retirer le métal atteint par polissage (retrouvez ici tous les équipements de polissage). Ce procédé est radical, mais il sacrifie inévitablement une part de l’objet.
Les taches de feu ne concernent pas uniquement l’argent 1er titre. Sur d’autres alliages, l’oxydation forme d’abord une couche d’oxyde de cuivre en surface. Mais juste en dessous, la zone s’appauvrit en cuivre, ce qui permet à l’oxygène de s’infiltrer davantage et de provoquer, là aussi, une oxydation interne.
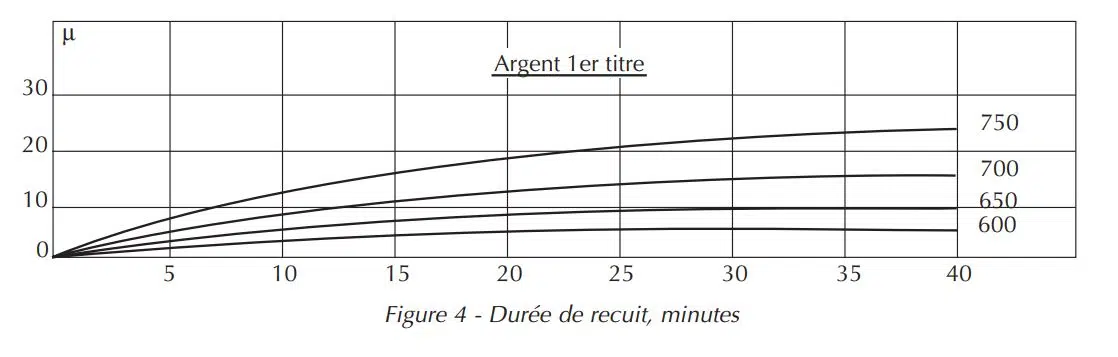
Après décapage, la surface qui réapparaît n’a souvent plus l’éclat d’origine, elle est terne, mate. La Figure 4 montre la progression de l’oxygène dans un alliage d’argent deuxième titre recuit à l’air, selon la température et la durée. On constate que la vitesse de formation des taches de feu y est plus faible qu’avec l’argent 1er titre.
Un autre point à surveiller : imaginons un alliage d’argent deuxième titre, oxydé puis décapé. Il se retrouve recouvert d’une fine couche d’argent pur, où sont piégés des grains d’oxyde de cuivre. Cette couche laisse passer l’oxygène très facilement. Si l’on recuit à nouveau sans qu’une nouvelle couche d’oxyde ne bloque le contact avec l’air, l’oxygène se diffuse rapidement dans cette zone superficielle avant d’être stoppé par l’alliage sous-jacent, plus riche en cuivre. Une couche d’oxygène se retrouve alors enfermée entre la surface appauvrie en cuivre et l’alliage interne. À première vue, le métal paraît impeccable. Mais il en faut peu pour que la couche d’argent pur se détache, révélant soudain la couche noire cachée en dessous.
L’oxydation revêt donc de multiples visages. Sa compréhension ne relève pas seulement de la théorie : elle guide les choix quotidiens des professionnels de la bijouterie, et motive de nombreux travaux de recherche.
Nous avons volontairement simplifié certains aspects, pour donner une vision concrète de ces phénomènes et permettre à chacun d’anticiper, voire de corriger, les surprises que réserve le travail des métaux précieux. Pour aller plus loin, contactez-nous : chaque atelier a ses questions, chaque alliage ses réactions.